发布时间:2025-04-25 14: 53: 00
PCR技术已经是分子生物学实验室中最常用的工具之一,PCR的成功率很大程度上取决于引物的设计质量。使用Oligo软件设计PCR引物时,很多实验人员都会特别关注引物之间是否容易形成二聚体,因为二聚体的形成会严重影响PCR扩增效率和特异性。但在实际操作中,很多朋友都对Oligo怎么评估引物二聚体形成,以及Oligo软件如何避免二聚体存有疑问。今天我们就围绕这些问题详细讲一讲,帮你更高效地完成引物设计,提升PCR实验的成功率。
一、Oligo怎么评估引物二聚体形成?
引物二聚体(Primer Dimer)指的是两个引物分子之间通过碱基互补形成的稳定复合物,一旦在PCR反应中形成二聚体,就会消耗引物,降低扩增效率,甚至导致实验失败。因此,提前评估二聚体形成的可能性对引物设计来说至关重要。
下面我们详细介绍如何使用Oligo软件对引物二聚体形成情况进行准确评估:
第一步:输入引物序列
首先,打开Oligo软件后,进入“Analyze”模块,选择“Primer Analysis”。在出现的对话框里输入你设计好的正向和反向引物序列。
例如:
Forward primer: 5'-AGCTGACCTGAACTG-3'
Reverse primer: 5'-TCAGGTCAGCTAGGC-3'
输入完毕后点击确定进行分析。
第二步:启动二聚体预测功能
引物序列输入完成后,在Oligo的分析界面中,选择菜单栏的:
Analyze → Duplex Formation(双链形成)
这个功能会自动评估你输入的两个引物之间可能形成的二聚体结构。
第三步:结果判读
Oligo完成分析后,会给出一个详细的二聚体评估报告,其中包括:
二聚体形成的概率(或稳定性)
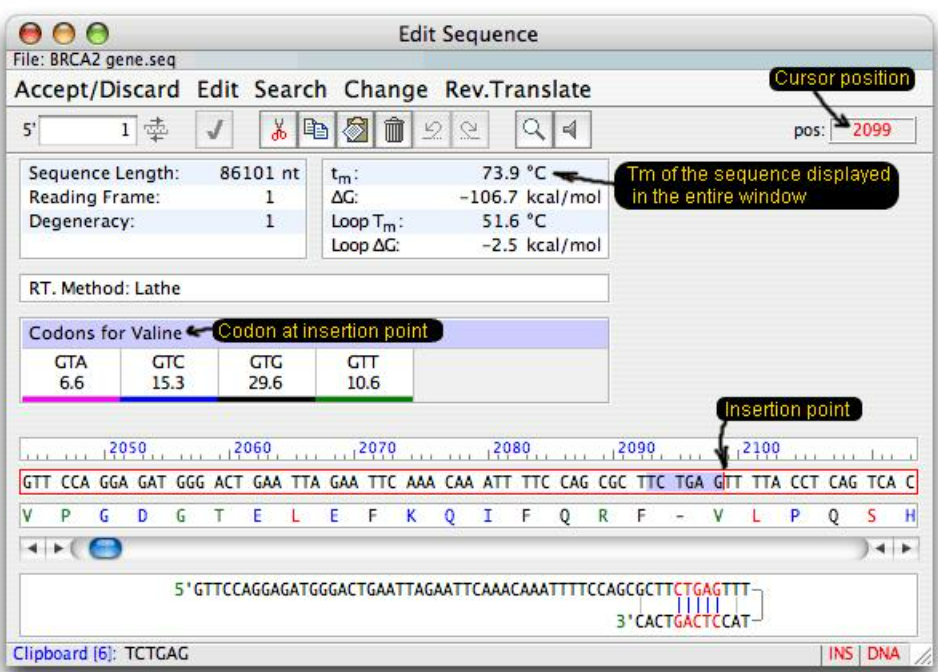
可能形成的二聚体结构图
二聚体的ΔG值(自由能变化)
一般来说:
ΔG值(自由能)越低(负值越大),二聚体越稳定,形成概率越高;
如果ΔG值小于-6 kcal/mol,说明二聚体形成风险较高,需重新设计或优化引物;
如果ΔG值在-3 kcal/mol以上(接近0),则说明风险很小,可以放心使用。
通过以上方法,你就能直观看出引物是否容易形成二聚体,并决定下一步是否需要优化引物设计。
二、Oligo软件如何避免二聚体?
当我们发现引物容易形成二聚体时,如何有效避免呢?Oligo软件提供了很多实用功能,帮助我们降低二聚体形成的风险:
1、改变引物序列位置
调整引物序列在模板DNA上的位置,避开与另一条引物形成互补的区域;
尽量避免引物3'端与另一条引物互补,这是形成二聚体最重要的原因之一。
2、调整引物长度和碱基组成
适当延长或缩短引物长度,使两个引物之间不再形成强互补区域;
避免3'端连续互补碱基,一般建议3'端至少连续3个碱基不与另一条引物互补。
例如:
将原引物:
5'-AGCTGACCTGAACTG-3'
改成:
5'-AGCTGACCTGAACAG-3'
稍作修改后可能就避免了二聚体的形成。
3、利用Oligo的“优化设计”功能
Oligo软件提供了自动优化设计功能,你可以直接使用:
Design → Optimize Primers(优化引物)
Oligo会自动尝试调整引物的序列、长度或位置,以最大程度降低二聚体形成概率。优化完成后再次进行二聚体评估,就能直观看到效果了。
4、调整引物退火温度(Tm)
提高引物的退火温度也能减少二聚体形成,因为较高的退火温度下,引物之间的弱互补配对不易稳定存在:
引物设计时,尽量选择Tm值在58-65℃之间;
提高退火温度后,引物特异性提高,引物与模板之间结合更加稳定,从而降低引物与引物之间的非特异结合概率。
5、使用二聚体形成最低的引物组合
如果设计多个备选引物,可以利用Oligo的批量分析功能:
Analyze → Batch Primer Analysis(批量引物分析)
一次性评估多 对引物组合,选择二聚体形成概率最低的引物对进行实验,确保PCR的成功率。
三、引物二聚体对PCR实验的影响
二聚体形成并非只是简单的影响扩增效率,还可能带来以下严重后果:
1、非特异扩增严重:二聚体存在时,PCR反应中会生成非特异片段,导致电泳条带模糊不清;
2、引物大量消耗:二聚体的形成导致引物被大量浪费,真正参与扩增的引物减少,影响扩增效率;
3、实时荧光定量PCR异常:如果是定量PCR,二聚体形成将造成Ct值异常,严重影响数据准确性。
因此,预防引物二聚体形成是PCR设计过程中至关重要的环节。
总结
今天我们详细讨论了Oligo怎么评估引物二聚体形成,也介绍了具体的操作步骤以及如何使用Oligo软件避免二聚体的方法。通过合理的引物优化和Oligo软件的科学评估,绝大部分引物设计中常见的问题都能有效避免。本文的内容能够帮助你在PCR实验中更高效地完成引物设计,减少引物二聚体的干扰,让实验成功率和稳定性大大提升。
展开阅读全文
︾
读者也喜欢这些内容:
Oligo引物二聚体太多怎么办 Oligo二聚体阈值怎么调整
Oligo引物二聚体太多怎么办,Oligo二聚体阈值怎么调整,通常是设计筛选口径偏松或引物末端互补性过强叠加导致的结果。你要做的不是只盯着一条ΔG数值,而是先把二聚体类型分清,再把Oligo里用于筛选的阈值设到与你的PCR体系匹配,同时把容易长二聚体的序列位置改掉,最后用软件窗口把实际二聚体配对形态复核一遍。...
阅读全文 >
Oligo引物二聚体怎么避免 Oligo二聚体检查如何分析解决
在分子生物学实验中,PCR扩增效率和特异性直接受到引物设计质量的影响,其中最常见的问题之一就是引物二聚体的形成。为了解决Oligo引物二聚体怎么避免,Oligo二聚体检查如何分析解决这一关键性问题,本文将系统解析Oligo软件在引物二聚体预测、避免与修正方面的应用策略,并结合具体操作流程与实用技巧,帮助科研人员高效规避该类设计隐患。...
阅读全文 >
Oligo软件预测引物二聚体 引物二聚体对测序的影响
在分子生物学实验中,引物设计是PCR成功与否的关键步骤之一。尤其是在高通量测序、qPCR等敏感实验中,引物二聚体的形成会显著干扰扩增效率和测序质量。本文围绕Oligo软件预测引物二聚体,引物二聚体对测序的影响展开,详细说明如何利用Oligo软件高效判断潜在二聚体结构,并解析引物二聚体对实验结果造成的实际影响。...
阅读全文 >
Oligo软件如何统计序列信息 Oligo怎么导出统计结果
在分子生物学的研究与实验中,对序列的统计分析是一项非常基础却关键的工作。无论是GC含量、碱基组成,还是序列长度与熔解温度(Tm),这些统计信息都直接影响到引物设计、克隆构建、合成策略等各个方面。Oligo软件如何统计序列信息Oligo怎么导出统计结果,成为许多科研人员在实际操作中经常遇到的需求。本文将围绕这个主题,详细介绍Oligo软件中与序列统计相关的核心功能、使用方法和结果导出技巧,帮助用户更高效地获取并利用这些关键数据。...
阅读全文 >