发布时间:2025-07-31 08: 00: 00
在分子生物学实验中,逆转录是将RNA转录为cDNA的重要步骤,而引物的选择直接决定了逆转录的效率和特异性。“Oligo引物和random引物区别,Oligodt和随机引物作用一样吗”是实验新手和科研人员经常关注的问题。无论是在qPCR、RNA测序还是文库构建前期,引物选择都会影响到后续分析的可靠性和数据一致性。为了更好地理解这两个引物类型的差异及其在实验中的应用效果,本文将通过三个层面详细分析,并补充扩展一类常见但易被忽视的引物——基因特异性引物。
一、Oligo引物和random引物区别
在逆转录反应中,Oligo和random引物是两种最常用的启动方式,它们的构造和作用机制存在本质差异:
1.结构与组成不同
Oligo引物通常指Oligo,是一段由连续的dT碱基组成的寡核苷酸,能够与mRNA分子3'端的poly(A)尾巴特异性结合。而random引物是由多个随机排列的六核苷酸组成,可在整个RNA分子上随机结合,启动多个位置的cDNA合成。
2.结合区域不同
Oligo只能结合于真核生物mRNA3'端的poly(A)尾部,因此合成的cDNA起点固定,生成的cDNA较长,完整性较高。random引物则可随机结合于mRNA、rRNA或其他RNA分子中间或靠前位置,生成的cDNA长度不一,更适合模板退化较严重的样本。
3.适用场景不同
Oligo引物适用于质量较好的mRNA样本,适合qPCR、文库构建、表达谱分析等需要反映mRNA整体结构的实验。而random引物更适合降解样本或需要捕获非poly(A)尾mRNA的实验,如某些病毒RNA、不带poly(A)尾的原核生物mRNA、或用于探索lncRNA。
4.产物种类与比例差异
使用Oligo引物可特异性地合成mRNA的cDNA,rRNA和tRNA几乎不会被转录。而random引物由于不区分RNA类型,往往会引入rRNA、lncRNA等非目标产物,可能对后续数据分析产生噪声。
通过以上对比可见,Oligo引物和random引物并非互相替代,而是根据实验目标来灵活选用的工具。
二、Oligo dt和随机引物作用一样吗
许多实验新手在操作时会问:既然Oligo(dT)和random引物都能用于cDNA合成,它们的作用是不是等价的?答案是否定的。两者虽然都能启动逆转录反应,但在合成产物的长度、代表性和应用精度方面有显著差别:
1.逆转录效率与均一性差异
Oligo(dT)在结合poly(A)尾后启动逆转录反应,生成的cDNA覆盖的是从3'端开始延伸的完整mRNA片段,代表性强,适合表达定量。但在部分降解的RNA样本中,若poly(A)尾被截断,则可能导致反应失败。
随机引物能在多个位置启动反应,虽然cDNA碎片较短,但更容易获取不完整的模板信息。因此在RNA质量偏低或存在裂解的样本中,使用随机引物更稳妥。
2.在qPCR和文库构建中的表现
Oligo(dT)在qPCR中更具优势,因其转录产物完整、长度适中,有助于保证定量准确性。而在RNA-Seq等需要覆盖广泛转录本的文库构建中,常常选择random hexamers,以提高覆盖度并减少偏好性。
3.特异性与非特异性产物比例
使用Oligo(dT)时,大多数情况下只转录poly(A)尾的真核mRNA,因此更适合聚焦于编码基因的分析。random引物则可能导致非特异性扩增,引入rRNA等背景产物,因此需要结合rRNA去除步骤。
4.组合使用以提升效率
在某些商业试剂盒或高级实验中,常常将Oligo(dT)和random引物混合使用,以兼顾全覆盖和特异性。例如用50% Oligo(dT)和50% random hexamers混合,可以既获得完整转录本,又补足部分降解区域。
综上所述,Oligo(dT)和random引物虽然目标相似,但在具体反应中的行为、产物特性和适用情景均存在显著差异,应根据实验目的和样本状态谨慎选择。
三、基因特异性引物在Oligo引物使用中的补充作用
除了常规的Oligo(dT)和random hexamers,科研中还经常用到“基因特异性引物,这类引物是专门针对目标基因设计的一段DNA序列,可以精准启动逆转录反应,在某些应用场景中具有不可替代的价值:
1.针对性强,避免背景干扰
GSP与目标mRNA互补,仅启动该基因的cDNA合成,特别适合低丰度mRNA、病毒RNA或不具poly(A)尾的转录本。结合Oligo软件设计GSP时,需特别注意GC含量、退火温度、二聚体结构等参数。
2.适用于快速诊断或特定通路分析
在某些快速检测实验或通路验证中,只需要检测某个基因的表达水平,使用GSP能显著提高反应效率与特异性,避免背景RNA影响结果。
3.步骤设计参考
使用Oligo软件导入目标mRNA序列;
设置设计范围覆盖目标外显子;
分析Tm值与二聚体风险;
合成引物后在逆转录反应中替代Oligo(dT)或random hexamers加入,即可专一性反转录。
4.限制与注意事项
GSP不能生成全长cDNA,因此不适合文库构建或未知转录本研究。且由于只捕获单个目标,需确保引物设计无偏差。
基因特异性引物作为Oligo体系下的一种精准策略,尤其在病毒检测、低表达基因分析中展现出极高的应用价值。
展开阅读全文
︾
读者也喜欢这些内容:
反转录过程中常用的引物有哪几类 反转录用随机引物还是olig
在RNA研究与转录组分析中,反转录是基础又关键的一步,它将RNA模板转录成cDNA,为后续PCR扩增、qPCR定量、RNA测序等实验打下基础。实验结果的准确性与反转录使用的引物类型有密切关系。因此,“反转录过程中常用的引物有哪几类,反转录用随机引物还是oligo”成为科研工作者特别关注的问题。本文将围绕这两个核心主题展开详细说明,以提升实验效率与数据质量。...
阅读全文 >
引物设计的原则有哪些 如何用Oligo软件设计引物
引物设计在分子生物学实验中至关重要,尤其在PCR扩增、测序、突变分析等场景中,一对高质量的引物往往决定整个实验是否成功。面对复杂的基因组信息与实验需求,科学合理地设计引物成为每个科研人员必备的技能。Oligo软件作为专业的引物设计工具,因其高精度、参数可控、结构分析功能强大,在科研工作中被广泛应用。本文围绕“引物设计的原则有哪些,如何用Oligo软件设计引物”这一主题,深入讲解引物设计的核心原则、Oligo操作方法,帮助科研人员提高实验效率和数据可靠性。...
阅读全文 >
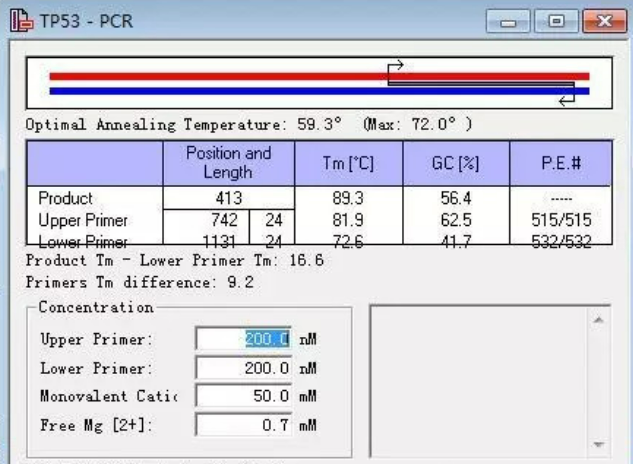
Oligo软件如何导出数据到Excel Oligo的导出格式怎么选择
在使用Oligo软件进行引物设计和序列分析时,导出设计结果是一个非常关键的步骤。无论是用于记录、项目归档,还是后续进行实验排版、报告整理,很多用户都希望能将Oligo中的数据直接导出为Excel格式,便于整理和共享。而这就引出了两个核心问题:Oligo软件如何导出数据到Excel,以及Oligo的导出格式怎么选择。本文将从实际操作、格式解析和使用建议等方面,为你详细讲解这一过程。...
阅读全文 >
Oligo软件如何模拟测序结果Oligo的测序模拟怎么操作
在分子生物学研究中,PCR引物设计和测序分析是两个关键环节。而Oligo软件不仅在引物设计方面功能强大,还具备一定的测序模拟能力,能帮助科研人员预估实验结果、避免设计错误。那么,Oligo软件如何模拟测序结果Oligo的测序模拟怎么操作?本文将围绕这一主题,深入讲解Oligo测序功能的使用场景、操作步骤与注意事项,助你高效开展分子实验设计。...
阅读全文 >