发布时间:2025-03-30 09: 00: 00
今天再来说说大家很关注的一个问题:Oligo软件如何评估引物灵敏度 引物的灵敏度怎么测试,还有在实际实验里,怎么才能测一下引物灵敏度,这篇文章将给你详细介绍一下这两个问题,让你看完就能学会!
一、Oligo软件如何评估引物灵敏度?
灵敏度就是引物能检测到目标模板的最低数量或者最低浓度的能力。也就是说,引物灵敏度越高,在PCR时,模板量即使非常少也能清楚地扩增出来。
不过要先说明一下,Oligo软件本身并不会直接给你一个叫做“灵敏度”的评分,它更注重引物的特异性、扩增效率这些方面。但我们可以通过Oligo评估的一些关键参数,间接判断出这对引物的灵敏度大概会怎样。
那么在Oligo软件里,哪些因素跟引物灵敏度有关呢?
① 引物的Tm值(熔解温度)
Oligo软件计算的Tm值,直接影响PCR反应时的退火效率。一般来说,引物的Tm值控制在55-65℃之间,且两个引物的Tm值差异在2℃以内,扩增的灵敏度通常就比较高。
② 引物的GC含量和序列结构
GC含量在45%-55%时,引物和模板结合更加稳定,更容易实现低浓度模板的高效扩增。Oligo软件还会检查引物序列有没有复杂的二级结构,比如发夹结构或二聚体。引物序列结构简单,不易形成二聚体或发夹结构,灵敏度自然就高。
③ 引物的特异性评分(Specificity Score)
Oligo软件自带特异性评分功能,如果引物特异性评分高,说明引物和目标序列匹配得特别好。特异性高的引物,PCR扩增时非特异性扩增少,灵敏度通常也会更高。
Tm值适中且稳定GC含量合理特异性评分高、二级结构少
满足这些条件的引物,一般灵敏度都会比较高。
二、引物的灵敏度怎么测试?
虽然软件能帮我们设计出高灵敏度的引物,但实验室做实验还是需要实际测一下,引物到底能扩增多低浓度的模板。这里教大家最常用的一个方法,就是梯度稀释法(Serial Dilution Method)。
具体怎么操作呢:
第一步:准备高浓度模板DNA或标准品
首先你需要一个高浓度、纯度好的DNA模板,比如PCR产物、质粒DNA或者基因组DNA。
第二步:进行系列梯度稀释
用无菌水或TE缓冲液,把DNA模板做10倍系列稀释,比如:原液浓度:100 ng/µL → 10 ng/µL → 1 ng/µL → 100 pg/µL → 10 pg/µL → 1 pg/µL一般建议稀释5-7个浓度梯度,涵盖从高浓度到极低浓度的范围。
第三步:进行PCR扩增实验
用你要测的引物,对每个梯度浓度的模板分别进行PCR扩增。注意PCR条件(循环数、退火温度、引物浓度等)要严格一致,这样结果才准确。
第四步:跑胶或者荧光定量分析扩增结果
PCR做完后,用琼脂糖凝胶电泳跑胶看看产物是否清晰可见。如果你用的是荧光定量PCR,则更容易准确判断,引物灵敏度看Ct值(循环阈值),Ct值越低,表示引物灵敏度越高。
怎么判断灵敏度结果?
引物能够扩增出的最低模板浓度,就是它的灵敏度界限。比如:你发现1 pg/µL模板依然能扩增清晰的条带或较低的Ct值,那说明你的引物灵敏度非常好。
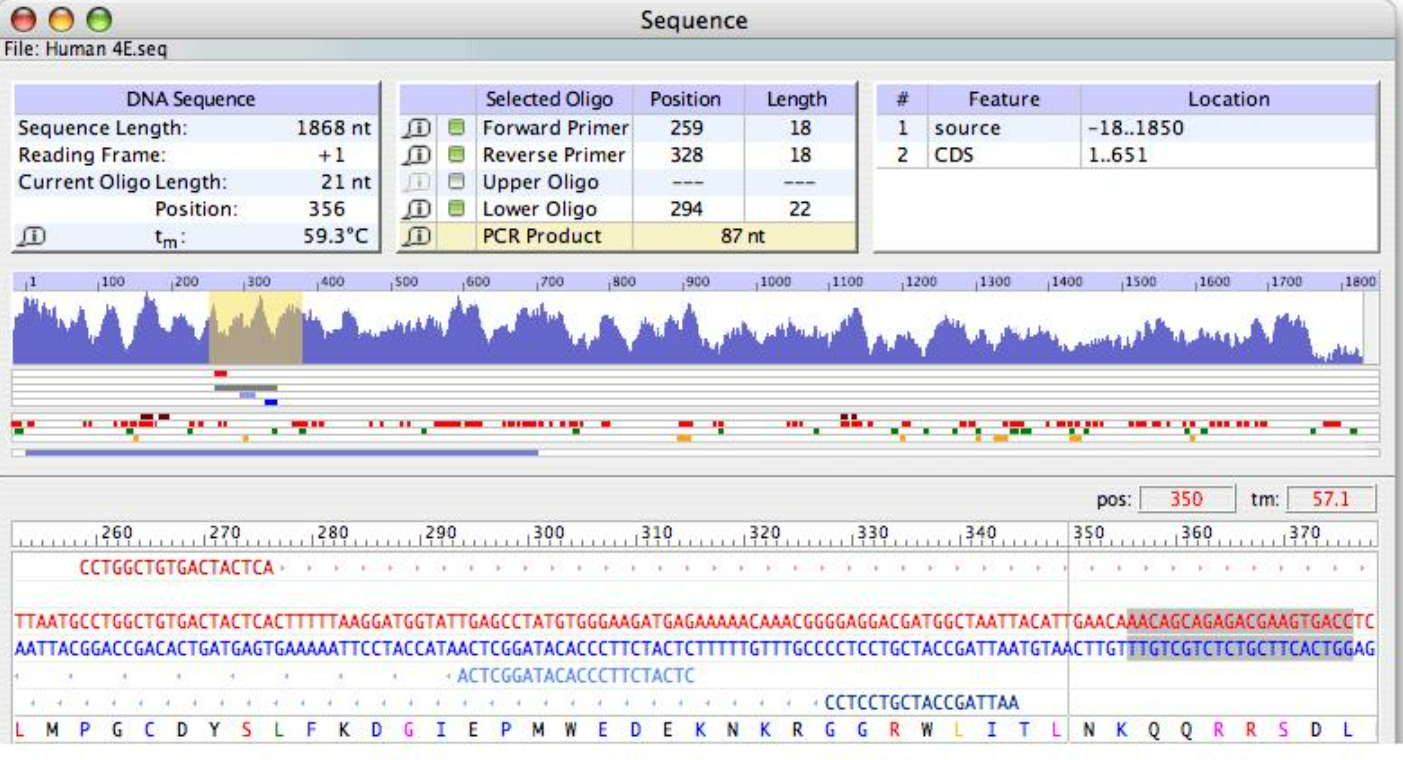
三、如何进一步提高引物灵敏度?
如果你测了之后发现引物灵敏度不太理想,还有几个小技巧可以帮你进一步提高:
① 优化PCR反应体系
增加PCR循环数(比如从30个循环增加到35个),可以检测更低浓度模板。适当调整退火温度(比如稍微降低1-2℃),更容易结合低浓度模板,提高扩增灵敏度。
② 提高模板纯度和质量
模板越干净,PCR灵敏度越高。如果模板纯度不好,扩增灵敏度会明显下降。可以再纯化一下你的DNA模板,比如再用试剂盒纯化一遍。
③ 调整引物浓度和Mg²⁺浓度
适当提高一点引物浓度(0.2-0.5 µM),或者稍微提高一下Mg²⁺浓度(2-2.5 mM),都能明显提升扩增灵敏度。
④ 选择高质量的PCR试剂
选择一些高灵敏度PCR试剂,比如高保真聚合酶或者高效荧光定量PCR Mix,能明显提高引物扩增灵敏度。
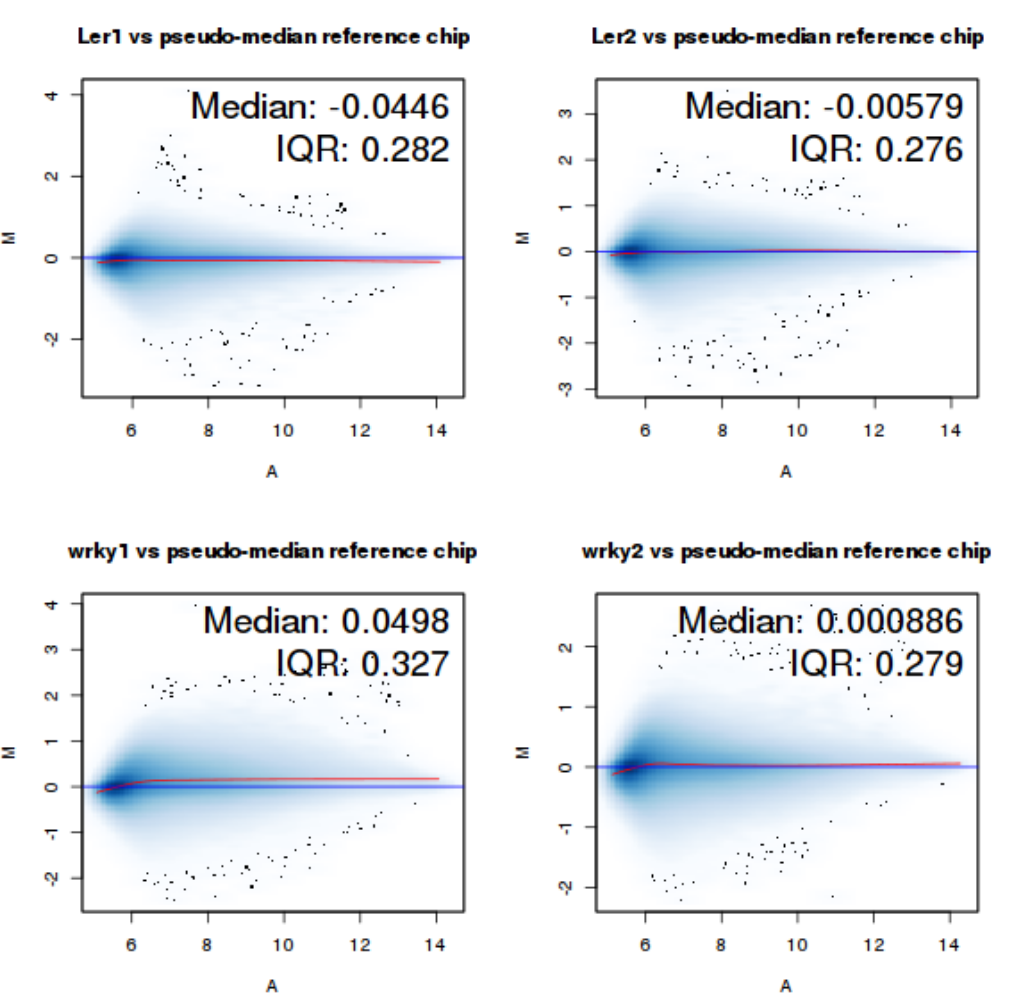
总结
今天咱们详细聊了Oligo软件如何评估引物灵敏度 引物的灵敏度怎么测试,虽然软件不直接显示灵敏度,但可以通过Tm值、GC含量和特异性评分间接判断,还提供了提高灵敏度的一些实用小技巧,这些都可以让你的PCR扩增更加精准高效。
展开阅读全文
︾
读者也喜欢这些内容:
Oligo引物设计软件准确吗 Oligo引物设计结果如何验证特异性
在现代分子生物学实验中,引物设计质量直接影响实验的特异性、敏感度及扩增效率。Oligo作为一款专业的寡核苷酸设计工具,其在引物筛选、二级结构预测和特异性控制方面的功能被广泛认可。围绕Oligo引物设计软件准确吗,Oligo引物设计结果如何验证特异性这一主题,本文将从软件算法与实践效果两个角度出发,系统剖析Oligo的核心优势与应用方法,并拓展介绍如何在不同实验场景下进一步优化引物性能,提升整体实验成功率。...
阅读全文 >
Oligo引物和random引物区别 Oligo dt和随机引物作用一样吗
在分子生物学实验中,逆转录是将RNA转录为cDNA的重要步骤,而引物的选择直接决定了逆转录的效率和特异性。“Oligo引物和random引物区别,Oligodt和随机引物作用一样吗”是实验新手和科研人员经常关注的问题。无论是在qPCR、RNA测序还是文库构建前期,引物选择都会影响到后续分析的可靠性和数据一致性。为了更好地理解这两个引物类型的差异及其在实验中的应用效果,本文将通过三个层面详细分析,并补充扩展一类常见但易被忽视的引物——基因特异性引物。...
阅读全文 >
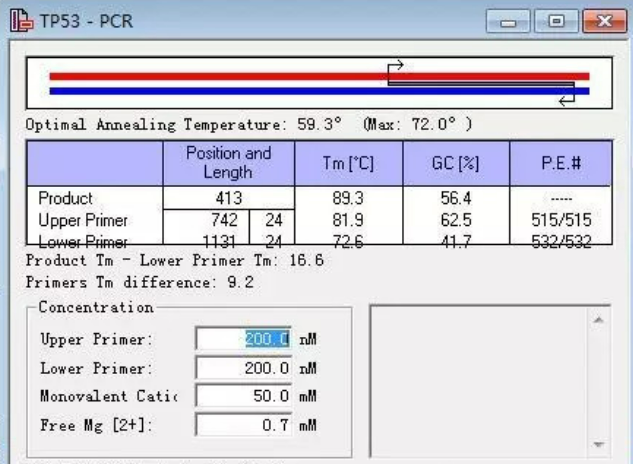
Oligo软件如何导出数据到Excel Oligo的导出格式怎么选择
在使用Oligo软件进行引物设计和序列分析时,导出设计结果是一个非常关键的步骤。无论是用于记录、项目归档,还是后续进行实验排版、报告整理,很多用户都希望能将Oligo中的数据直接导出为Excel格式,便于整理和共享。而这就引出了两个核心问题:Oligo软件如何导出数据到Excel,以及Oligo的导出格式怎么选择。本文将从实际操作、格式解析和使用建议等方面,为你详细讲解这一过程。...
阅读全文 >
Oligo软件如何评估引物交叉反应 怎么避免引物的交叉反应
在分子生物学实验中,PCR引物设计的准确性直接决定了扩增的特异性和效率。其中,“引物交叉反应”是一个经常被忽视却极易引发实验失败的技术细节。所谓交叉反应,指的是不同引物之间形成二聚体或者错误结合,导致非特异性扩增,进而影响实验结果的准确性。Oligo软件作为一款专业的寡核苷酸设计工具,具备强大的交叉反应预测与评估功能。本文将围绕“Oligo软件如何评估引物交叉反应”以及“怎么避免引物的交叉反应”两个实际问题展开,从原理、操作到优化策略,深入探讨PCR引物设计中的核心技巧。...
阅读全文 >