发布时间:2025-04-12 08: 00: 00
在分子生物学实验中,PCR技术是一项重要的基本技能,而成功的PCR反应,关键就在于引物设计的精准性。很多实验人员在设计引物时,都会用到Oligo软件,它能帮我们预测引物的各种特性,尤其是错配率(Mismatch Rate)的评估。然而,很多同学在实际使用过程中会遇到这样的问题:Oligo软件如何评估引物错配率,引物的错配率怎么降低? 今天我们就针对这两个问题,详细聊聊Oligo软件如何评估引物错配率 引物的错配率怎么降低,帮助你提高PCR反应的成功率。
一、Oligo软件如何评估引物错配率?
Oligo是一款功能强大的PCR引物设计工具,它不仅能计算引物的退火温度(Tm)、GC含量和二级结构,还能对引物的错配率进行精准评估。下面我们来详细说一下在Oligo中如何进行错配率评估:
第一步:导入待评估的引物序列
首先打开Oligo软件,进入主界面后,你需要输入你设计好的引物序列。比如在“Primer Analysis”(引物分析)或“Primer Search”(引物搜索)模块中输入序列。
输入好序列之后,点击确认,进入引物分析界面。
第二步:设置目标模板序列
错配率评估的关键是确定目标模板DNA序列。因此,在进行评估前,你需要将目标DNA模板序列导入到Oligo软件中,可以通过菜单栏的:
File → New Sequence
将目标模板序列输入到软件里,或者从已有的数据库文件导入进来。
第三步:执行引物错配率分析
在导入目标序列后,选择菜单栏上的:
Analyze → Primer Search
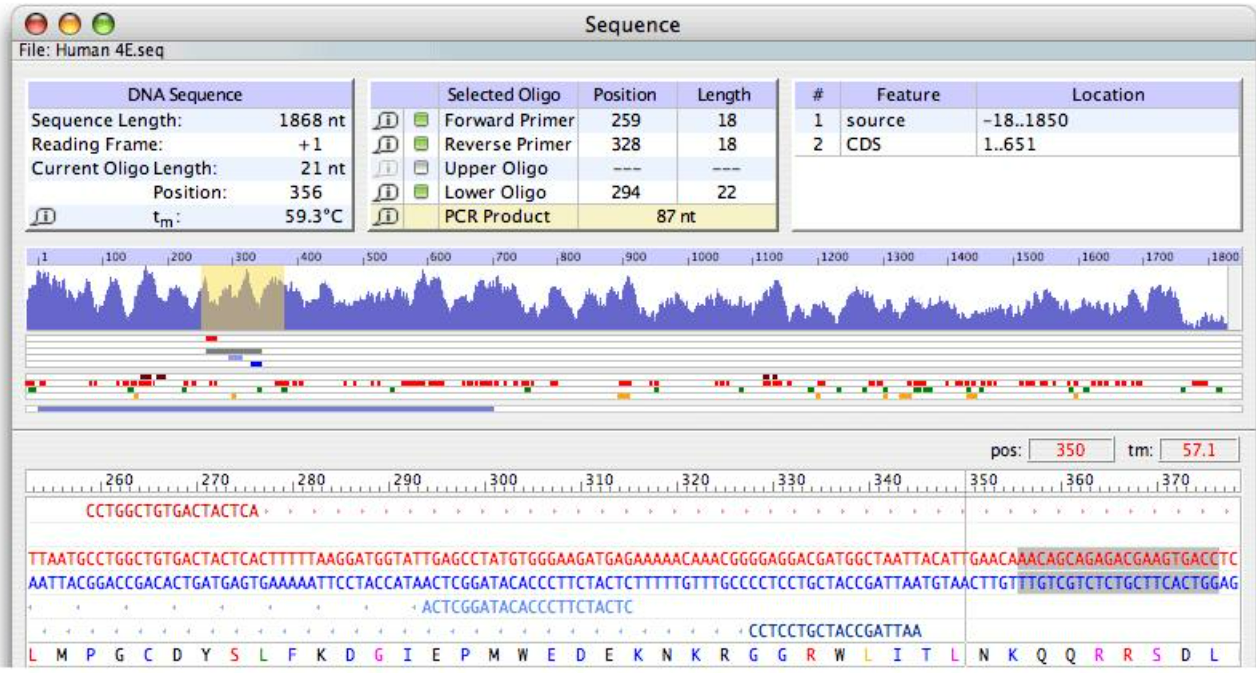
Oligo软件会自动将你设计的引物序列与目标模板序列进行比对,并快速计算出可能存在的错配位置和错配比例。
分析结果中会清晰显示出错配的位置,比如第几个碱基存在错配,以及总的错配率是多少。这些信息会让你快速判断引物与模板之间的结合稳定性,从而评估引物的设计质量。
第四步:结果判读
在Oligo给出的结果中,一般认为:
错配率越低越好,理想情况下建议小于5%。
若错配率超过10%,则说明引物可能出现较多非特异结合,后续PCR反应可能出现非特异扩增甚至失败。
根据Oligo的提示,你可以直观看出引物设计中的不足,及时优化调整。
二、引物的错配率怎么降低?
当发现引物的错配率较高时,我们如何有效地降低呢?下面给大家详细讲解一些实用技巧:
1、 重新优化引物长度和位置
引物错配经常出现在过短或者位置选择不理想的情况下。此时建议:
延长引物长度:稍微延长引物序列可以提高特异性,减少错配。
调整位置:将引物设计在模板序列中更保守、更特异的区域,避免选择重复序列或高GC含量区域。
2、 避免引物序列中易错配区域
模板序列中某些特定区域,比如重复序列或具有较高变异率的区域,很容易引发引物错配。设计引物时,应尽量避开这些区域:
尽量避开重复序列或回文序列区域;
选择进化保守的DNA片段区域作为引物结合位点,显著降低错配的概率。
3、 提高引物退火温度(Tm值)
提高引物退火温度能增加引物和模板之间的特异性结合:
选择Tm值更高一点的引物设计(一般推荐58-65℃之间);
提高退火温度可有效减少引物与非目标序列的非特异结合,从而降低错配。
4、 调整引物GC含量和末端碱基
适当提高GC含量:一般建议GC含量控制在40%~60%,适当提高可增强引物与模板的结合稳定性;
优化引物3'端碱基:引物3'端的碱基对PCR反应至关重要,避免3'端出现连续的A/T碱基,更倾向于选择G/C碱基作为末端,能明显降低错配概率。
⑤ 使用Oligo再次分析与验证
调整引物序列后,务必再次用Oligo重新评估错配率。如果仍然不理想,就继续进行微调,反复验证直至达到满意的错配率范围。
三、引物错配率高对PCR的影响
了解错配率的意义,对PCR实验非常重要。一般来说,高错配率的引物可能会导致以下问题:
1、PCR产物特异性差:容易产生非特异扩增,出现多条扩增条带;
2、扩增效率降低:错配的引物结合不稳固,会严重影响扩增效率;
3、PCR产物难以测序:若错配严重,即使得到扩增产物,也会影响后续测序的准确性,导致实验失败。
因此,降低错配率不仅仅是提高PCR成功率的关键,也是保障后续分子生物学实验顺利进行的重要环节。
总结
通过今天的详细讲解,相信你已经清楚地了解了Oligo软件如何评估引物错配率,也掌握了有效降低引物错配率的方法。使用Oligo设计并评估PCR引物时,要遵循科学合理的方法,多次优化调整,确保每次PCR反应都能达到理想的效果。
展开阅读全文
︾
读者也喜欢这些内容:
Oligo发卡结构检测有效吗 Oligo发卡结构如何避免优化
在引物设计与寡核苷酸合成的实践中,发卡结构的形成往往是导致反应失败或效率降低的关键因素。Oligo软件作为一款专业的引物分析与设计工具,其在识别和预测发卡结构方面的功能备受用户关注。围绕Oligo发卡结构检测有效吗,Oligo发卡结构如何避免优化的话题,本文将深入分析Oligo对发卡结构的识别机制、如何有效规避其形成,以及在实际工作中可以进一步扩展的优化建议,帮助科研用户提高实验成功率与设计效率。...
阅读全文 >

Oligo软件如何查找特定序列 Oligo的查找功能怎么使用
在日常的引物设计与分子生物实验中,精准定位特定序列是一项不可或缺的能力。对于使用Oligo软件的科研人员来说,如何快速查找目标DNA或RNA序列,不仅关系到设计效率,更影响到实验的可重复性和科学性。因此,本文将围绕“Oligo软件如何查找特定序列Oligo的查找功能怎么使用”这一主题,深入解析Oligo软件提供的查找功能使用方式及其高效策略。...
阅读全文 >
Oligo软件如何合并多个项目 Oligo合并项目后数据会冲突吗
在生物信息学分析和分子生物学实验设计中,Oligo软件是一款非常常用的引物设计与管理工具。当研究工作涉及多个实验批次或不同项目组合作时,常常需要将多个Oligo项目文件合并到一个统一的数据集中,便于统一管理、批量导出和数据备份。这时候,“Oligo软件如何合并多个项目Oligo合并项目后数据会冲突吗”这个问题就成了很多实验室人员和科研工作者在使用过程中必须解决的关键步骤。...
阅读全文 >
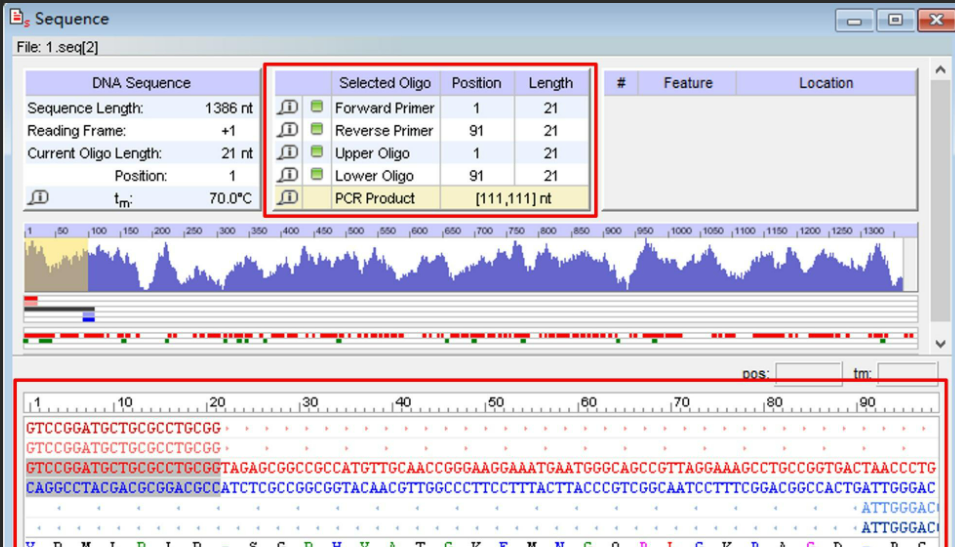
Oligo如何模拟PCR反应 Oligo的PCR反应模拟结果准确吗
在日常分子实验中,PCR(聚合酶链式反应)被广泛应用于基因扩增、突变检测、引物验证等多个核心步骤,而设计合理的引物组合和预测PCR结果的表现,几乎决定了整个实验是否成功。为此,许多科研人员开始依赖专业软件进行模拟预测,其中Oligo软件以其精确的分析能力和详尽的参数设定,在PCR模拟方面表现尤为出色。本文将围绕“Oligo如何模拟PCR反应 Oligo的PCR反应模拟结果准确吗”这一话题,详细解析Oligo在PCR模拟功能上的使用方法、逻辑机制以及结果的可靠性与局限性,帮助你更加科学地规划实验设计。...
阅读全文 >