发布时间:2025-04-04 08: 00: 00
在分子生物学实验中,引物的退火温度(Annealing Temperature,简称Ta)是影响PCR成功与否的关键因素之一。退火温度过高,引物难以与模板结合,可能导致PCR扩增失败;温度过低,则可能产生非特异性扩增。因此,准确评估和设置引物退火温度十分重要。今天,我们就详细聊一聊:Oligo怎么评估引物退火温度 Oligo怎么设置引物退火温度,帮助大家快速掌握使用Oligo软件进行退火温度分析和优化的具体方法。
一、Oligo怎么评估引物退火温度
Oligo软件是实验室常用的引物设计工具,它可以快速准确地计算引物的退火温度。具体使用方法并不复杂,我们一步一步来操作。
1、打开Oligo软件,输入引物序列
首先,在Oligo软件主界面新建一个项目,进入序列输入窗口,把你设计好的引物序列粘贴或输入进去,一般序列长度在18-30个碱基之间。
2、初步计算引物的退火温度(Ta)
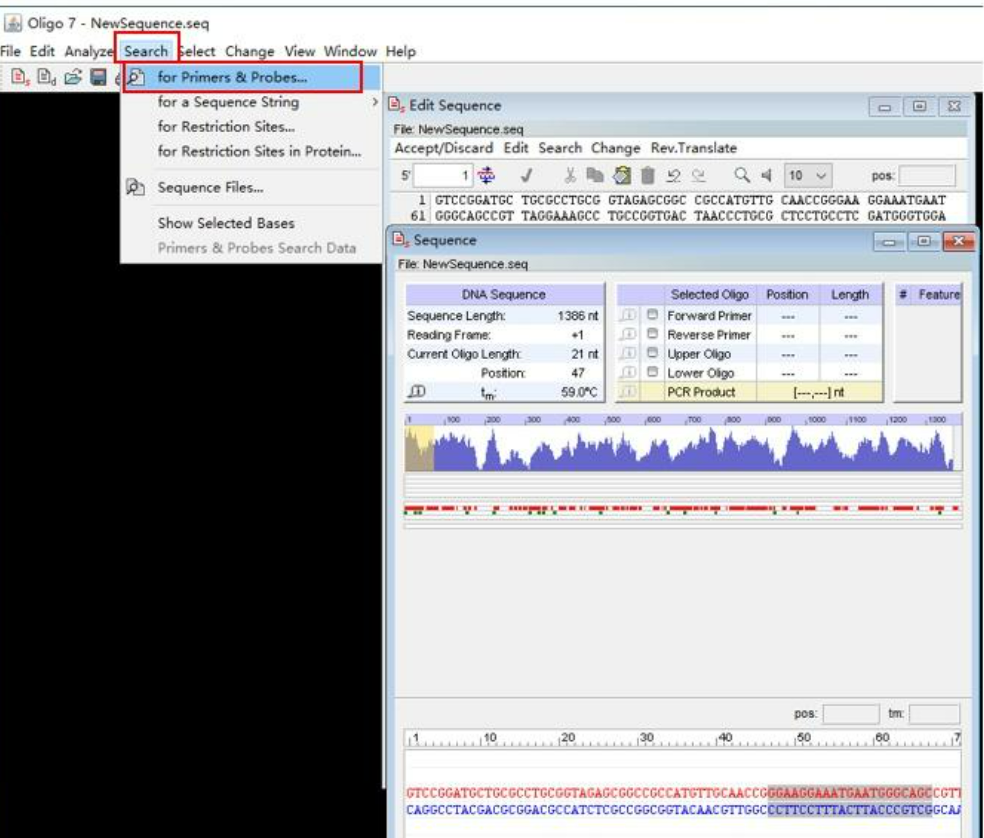
Oligo软件的分析功能非常全面,序列输入完毕后,软件会自动进行一些基础分析。你可以在界面顶部菜单中找到“Analyze”选项,点击后选择“Melting Temperature(熔解温度)”,软件会迅速显示当前引物的熔解温度(Tm)。
很多人会疑惑:退火温度和熔解温度(Tm)有什么关系?
其实,引物退火温度通常会略低于引物的Tm值,一般推荐设置在引物Tm值的3-5℃以下。因此,通过Oligo计算的Tm值,我们可以快速推算合适的退火温度。
举个例子,如果Oligo软件计算出的引物Tm值是58℃,那么你的退火温度(Ta)一般设定在53-55℃之间,通常取55℃左右就比较理想。
3、评估前后引物退火温度差异
如果是同时使用一对引物(正反引物),还需要注意一下两条引物的Tm值。Oligo软件也支持同时输入两条引物进行分析。
理想状态下,前后引物的Tm差距不超过2℃,这样可以确保两条引物同时高效退火。如果差距较大,则需要对其中一条引物序列做适当调整,比如增加或减少1-2个碱基,重新计算退火温度。
4、综合评估其他退火相关因素
Oligo软件不仅仅计算Tm值,还会自动分析引物的GC含量、二聚体和发夹结构倾向,这些因素也会影响实际的退火温度设定。
比如GC含量较高的引物,实际退火温度可能需要适当提高1-2℃;相反,GC含量较低的引物,实际退火温度可能需要略微降低。
二、Oligo怎么设置引物退火温度
当我们用Oligo准确评估出引物的熔解温度(Tm)后,下一步就是在实验中如何正确设置退火温度了。Oligo软件本身并不会直接“设置”退火温度,而是为你提供精准的分析数据,让你在PCR程序中更合理地设置Ta值。下面详细说明具体的实验操作方法:
1、根据Oligo给出的Tm值合理设定Ta值
一般来说,引物退火温度Ta值推荐设置为引物Tm值的3-5℃以下,常规PCR推荐设置为Tm-5℃,比如:
若Oligo计算的引物Tm值为60℃,则建议设置退火温度在55-57℃。
若Tm值为65℃,则退火温度设置在60-62℃最为合适。
2、梯度PCR验证法确定最优Ta值
虽然Oligo给出了退火温度的建议,但实际实验环境中,PCR仪器的温控精度、反应体系的不同,也可能导致实际最优的退火温度与理论值略有差异。
这时,我们可以使用梯度PCR的方式,围绕Oligo计算的Tm值进行梯度设置,如从Tm-8℃到Tm-2℃(比如Tm为60℃,设置52℃-58℃的梯度范围),一次PCR扩增多个不同退火温度,快速找到实验条件下的最优退火温度。
3、特异性和扩增效率评估
梯度PCR完成后,取少量PCR产物进行琼脂糖凝胶电泳,观察产物特异性、扩增效率(条带明亮度)以及是否存在非特异扩增的情况。
通过电泳条带表现,确定最为理想的退火温度。一般情况下,能在保证扩增产物特异性的同时获得清晰明亮条带的退火温度即为最佳值。
三、优化引物退火温度的小技巧
除了用Oligo软件评估退火温度和实验方法设置以外,这里再额外给大家分享一些提高PCR成功率的小技巧,帮助大家进一步优化引物退火温度的准确性:
1、精确计算Tm值的小技巧
在Oligo软件里,尽可能使用精确计算公式,比如Nearest-Neighbor算法(最近邻法),这个方法比一般简单公式更加精准,尤其适合高GC含量或较复杂的引物序列。
2、控制引物长度和GC含量
设计引物时,最好将引物长度控制在18-25bp之间,GC含量维持在40%-60%之间,避免出现连续的重复序列或过高GC含量,这样能获得更加稳定的退火条件。
3、前后引物Tm差异控制在2℃以内
若两条引物的退火温度差距超过2℃,应重新设计调整,引物对退火温度差距控制得越小,扩增的特异性和效率就越高。
4、PCR缓冲液和体系优化
如果引物退火温度已经很好,但扩增结果不理想,可以考虑优化PCR反应缓冲液、镁离子浓度等条件,比如适当提高Mg2+浓度可以增加引物与模板的结合稳定性。
总结
掌握了Oligo怎么评估引物退火温度 Oligo怎么设置引物退火温度,我们就能快速有效地确定和优化PCR实验中的退火条件,大大提高实验成功率。Oligo软件提供的准确Tm值计算和梯度PCR验证方法相结合,能够轻松找到实验条件下的最佳退火温度。再加上我们分享的一些小技巧,相信你能在实验室中更加高效地设计和完成PCR实验,顺利得到满意的结果。
展开阅读全文
︾
读者也喜欢这些内容:
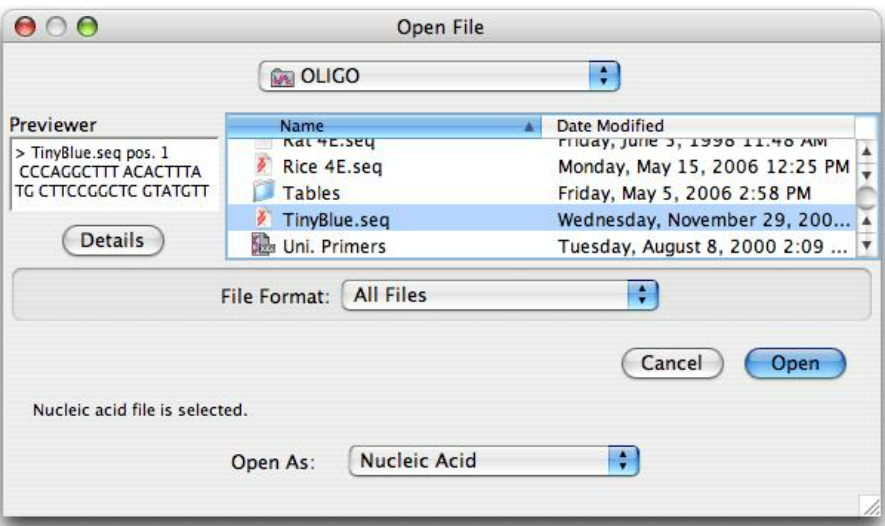
Oligo软件如何分析基因表达水平 Oligo如何评估表达水平
在基因功能研究与分子实验设计中,基因的表达水平往往决定了实验的成功率和结果解读的可靠性。尽管Oligo软件本质上是一款以引物设计为核心的工具,它并不直接测量基因表达量,但它却能通过优化寡核苷酸序列和分析结构参数,为我们间接评估和预测表达水平提供有力支持。本文将围绕Oligo软件如何分析基因表达水平 Oligo如何评估表达水平,系统讲解其应用逻辑、操作步骤以及结合实验的实用策略。...
阅读全文 >
Oligo软件如何预测RNA二级结构 Oligo的预测结果可靠吗
在分子生物学与核酸药物研究中,RNA二级结构的预测是分析转录后调控、RNA稳定性和靶向干扰效果的关键步骤。虽然Oligo软件最初是为寡核苷酸设计而开发,但它具备一定的RNA结构预测功能,特别在短链RNA结构稳定性分析、寡核苷酸靶向构型评估等方面具有实用价值。那么,Oligo软件如何预测RNA二级结构 Oligo的预测结果可靠吗?本文将从功能原理、操作步骤、结果解释以及适用范围等多个方面展开详细说明,帮助科研人员更合理地使用Oligo进行RNA结构分析。...
阅读全文 >
Oligo软件如何自动化序列分析 Oligo怎么设置自动化流程
在分子生物学的各类实验中,无论是进行PCR引物设计、探针开发,还是序列比对和特异性分析,自动化已成为提升效率和减少误差的关键手段。Oligo作为一款经典而专业的引物设计与序列分析软件,也提供了非常实用的自动化功能,可以帮助科研人员将多个任务串联起来,以批处理的方式完成重复性高、逻辑清晰的分析流程。围绕“Oligo软件如何自动化序列分析 Oligo怎么设置自动化流程”这一问题,本文将深入解析Oligo在自动化方面的核心功能、实际设置方法和应用技巧,助你在实验设计中更高效地应对复杂工作量。...
阅读全文 >
Oligo软件如何评估引物交叉反应 怎么避免引物的交叉反应
在分子生物学实验中,PCR引物设计的准确性直接决定了扩增的特异性和效率。其中,“引物交叉反应”是一个经常被忽视却极易引发实验失败的技术细节。所谓交叉反应,指的是不同引物之间形成二聚体或者错误结合,导致非特异性扩增,进而影响实验结果的准确性。Oligo软件作为一款专业的寡核苷酸设计工具,具备强大的交叉反应预测与评估功能。本文将围绕“Oligo软件如何评估引物交叉反应”以及“怎么避免引物的交叉反应”两个实际问题展开,从原理、操作到优化策略,深入探讨PCR引物设计中的核心技巧。...
阅读全文 >