发布时间:2025-05-28 14: 15: 00
在基因功能研究与分子实验设计中,基因的表达水平往往决定了实验的成功率和结果解读的可靠性。尽管Oligo软件本质上是一款以引物设计为核心的工具,它并不直接测量基因表达量,但它却能通过优化寡核苷酸序列和分析结构参数,为我们间接评估和预测表达水平提供有力支持。本文将围绕Oligo软件如何分析基因表达水平 Oligo如何评估表达水平,系统讲解其应用逻辑、操作步骤以及结合实验的实用策略。
一、Oligo软件如何分析基因表达水平
首先需要明确:Oligo并不直接测序或检测mRNA水平,但它通过以下几个维度,帮助科研人员在设计阶段预估目标基因的表达效率和转录表现。
1. 通过引物设计提高qPCR表达检测的灵敏度
Oligo可以设计qPCR、RT-PCR等定量实验中用于检测表达量的引物:
熔解温度(Tm)匹配合理,提升扩增效率;
避免形成二聚体、发卡结构,减少假阳性扩增;
跨外显子设计(exon-exon junction),避免基因组DNA干扰;
选择表达区域富集的区域(如3'UTR靠前区域);
通过这些精准设计手段,提高表达量检测的准确性与线性范围,从而间接帮助我们获取更稳定的表达数据。
2. 评估转录因子结合区的稳定性
表达的第一步是转录,而Oligo可用于分析启动子序列中:
是否存在TATA-box、CAAT-box等调控元件;
是否有合适的GC含量分布(40–60%更易于形成开放结构);
是否含有不利于表达的强发卡结构(二级结构越强越难被RNA聚合酶结合);
这些信息将帮助研究者判断一个基因是否具备良好的转录潜力,在设计合成启动子或筛选高表达片段时尤其重要。
3. 分析RNA二级结构影响翻译效率
Oligo提供自由能(ΔG)计算模块,可用于判断mRNA 5'端是否存在结构障碍;
例如强发卡结构可能阻碍核糖体扫描,影响表达;
可以使用Oligo比对不同突变或调控区的ΔG值,选择更利于表达的结构构型。
4. 辅助筛选高表达片段进行克隆表达
当你需要将基因克隆到表达载体中时,可以借助Oligo分析不同片段:
CDS(编码区)不同区域的表达效率预测;
剪接变体选择,找出稳定表达的mRNA形式;
不同片段的结构稳定性对比,辅助构建表达文库。
二、Oligo如何评估表达水平
接下来是通过Oligo实际评估表达相关因素的具体操作步骤。
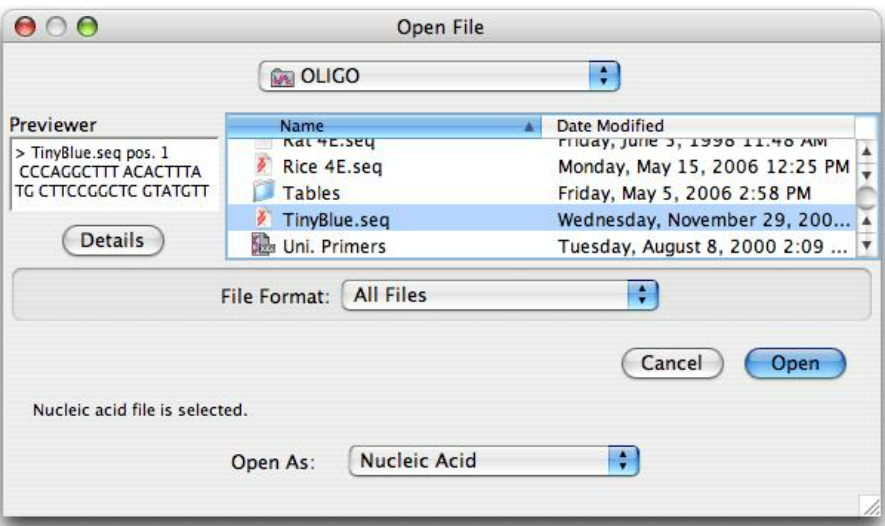
1. 导入目标基因序列
打开Oligo → “File → New Sequence”;
粘贴完整或截取的目标序列(如CDS、5'UTR、启动子);
设置序列属性为线性DNA,命名为“GeneX_Expression_Region”。
2. 分析序列的GC含量和结构
点击“Analyze → GC Content”:确认整体GC比例是否合理(过高或过低都会影响表达);
点击“Analyze → Self-Complementarity”:评估是否易形成不利结构,如发卡或自配对区域;
使用“ΔG Calculator”计算不同区段的自由能,数值越小说明结构越稳定,可能对表达造成干扰。
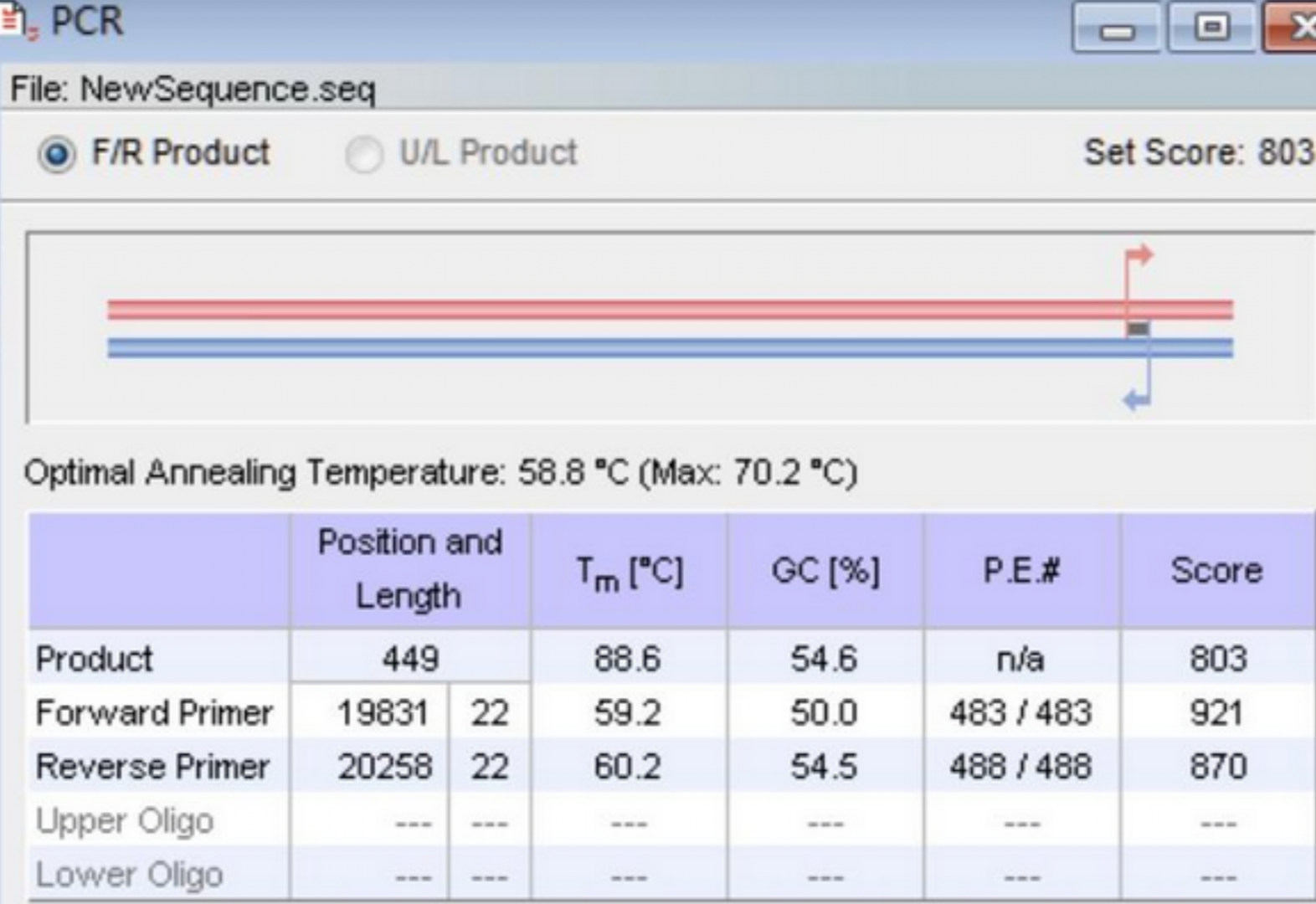
3. 引物设计辅助表达检测
选择“Primer Design → PCR Primer”模块;
输入你的目标区域,设定目标产物大小(如90–150bp用于qPCR);
检查每组引物的Tm值、GC含量、结构稳定性、跨外显子设计等;
保存最优引物序列,并用于后续qPCR实验测量表达量。
4. 启动子区域motif识别
使用“Motif Finder”手动设置搜索项(如“TATA”、“CAAT”、“GC box”);
评估这些核心调控元件的相对位置;
结合ΔG分析判断该启动子是否具备稳定的开放性结构,辅助判断其活性。
5. 比较不同变体表达预测值
若导入多个mRNA剪接变体或突变版本的启动子片段,可分别分析结构参数;
比较ΔG、self-complementarity、motif数量;
选择更稳定、motif集中、不易形成结构阻碍的序列作为高表达候选片段。
三、将Oligo分析结果与表达实验数据结合使用的建议
虽然Oligo不能直接输出“表达量高低评分”,但它提供的设计与预测结果,在下列实际应用中非常有价值:
1. 精准设计qPCR引物
通过Oligo事先设计高特异性、高效率的qPCR引物组,可以显著提升表达检测的准确性,尤其在检测微量RNA或miRNA表达时尤为重要。
2. 筛选适合构建表达载体的高表达序列
结合Oligo分析结果选择表达片段,可避免结构稳定性过高、翻译起始位置错误等问题,提高下游蛋白表达量。
3. 预测突变对表达的影响
有些点突变可能落在调控区或导致RNA结构突变,通过Oligo分析ΔG和结构模型变化,可以判断是否可能对表达产生上调或抑制效应。
4. 与后续实验平台衔接
Oligo设计的引物可无缝应用于qPCR、RT-PCR、RACE等实验流程;启动子结构分析结果也可用于进一步在CellDesigner、Benchling或合成生物软件中建模。
总结
虽然Oligo软件并不直接测量mRNA或蛋白表达量,但它能通过对核酸序列结构、热力学参数、调控元件识别等方面的综合分析,在基因表达预测与优化设计中扮演重要角色。本文围绕“Oligo软件如何分析基因表达水平 Oligo如何评估表达水平”系统介绍了其间接评估表达潜力的实用方法和具体操作技巧。
展开阅读全文
︾
读者也喜欢这些内容:
Oligo引物设计软件准确吗 Oligo引物设计结果如何验证特异性
在现代分子生物学实验中,引物设计质量直接影响实验的特异性、敏感度及扩增效率。Oligo作为一款专业的寡核苷酸设计工具,其在引物筛选、二级结构预测和特异性控制方面的功能被广泛认可。围绕Oligo引物设计软件准确吗,Oligo引物设计结果如何验证特异性这一主题,本文将从软件算法与实践效果两个角度出发,系统剖析Oligo的核心优势与应用方法,并拓展介绍如何在不同实验场景下进一步优化引物性能,提升整体实验成功率。...
阅读全文 >
Oligo软件如何导入外部数据库 Oligo支持哪些数据库
Oligo是一款广泛应用于引物设计、探针筛选及基因合成辅助的专业软件,凭借其高准确性和灵活的功能设置,在分子生物学、基因工程等领域拥有良好的口碑。在实际使用中,很多用户会希望将外部数据库中的序列、注释或物种信息导入Oligo软件中,以便进一步进行高通量的引物筛选或比对分析。那么,Oligo软件如何导入外部数据库Oligo支持哪些数据库,这两个问题也就成了用户经常关注的重点。下面就围绕这两个问题进行详细的讲解。...
阅读全文 >
Oligo软件如何管理序列数据 Oligo软件如何备份项目数据
在分子生物学实验设计中,序列数据的规范管理和项目的安全备份,是确保科研流程顺利进行的重要保障。尤其是在使用功能强大的Oligo软件进行引物设计、寡核苷酸分析、结构预测等工作时,若不做好数据管理与备份,一旦发生系统崩溃或数据丢失,后果将极为严重。本文将详细讲解Oligo软件如何管理序列数据 Oligo软件如何备份项目数据,帮助用户建立起稳定、高效、安全的科研数据处理流程。...
阅读全文 >

Oligo软件如何预测启动子活性Oligo的活性预测怎么操作
在分子生物学研究中,启动子区域的预测和分析对于理解基因调控、设计表达载体、构建合成生物回路都至关重要。而Oligo软件,作为一款经典的寡核苷酸设计工具,也提供了部分关于启动子活性预测的辅助功能。虽然它不是专门的转录因子结合位点分析软件,但在合理配置下,仍可用于启动子区域分析与活性预测前期的设计评估。本文将围绕Oligo软件如何预测启动子活性Oligo的活性预测怎么操作这一话题,为你系统梳理分析方法与操作技巧。...
阅读全文 >